抗体の複雑性の解明: 軽鎖、重鎖、定常領域、腫瘍関連抗原
コンテンツ
1. 抗体の概要
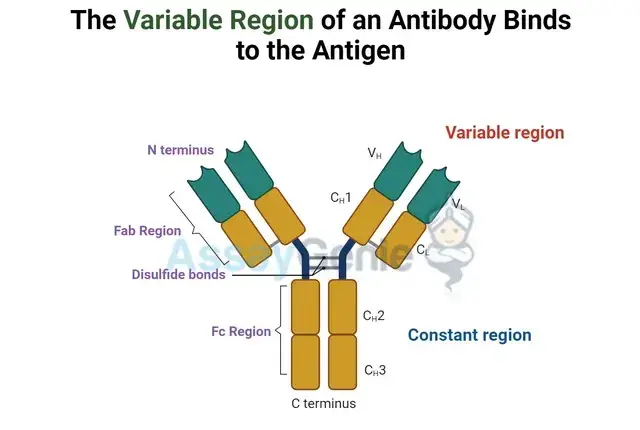
2. 抗体の構造
重鎖と軽鎖
抗体分子は、Fab (抗原結合) 領域と Fc (定常) 領域の 2 つの主要領域に分岐します。 Fab 領域は抗原認識を担当し、Fc 領域は細胞表面受容体および補体系との相互作用を媒介し、免疫応答に影響を与えます。

Fab 領域: 抗原認識の鍵
Fab (フラグメント抗原結合) 領域は抗体の防御戦略の最前線にあり、抗原の特異的な認識と結合を担当します。この領域は重鎖と軽鎖の両方 (VH と VL) の可変ドメインで構成され、これらが一緒になって独特の抗原結合部位を形成します。これらのドメインのアミノ酸配列の多様性により、抗体の多様なレパートリーが可能になり、それぞれが特定の抗原エピトープに結合することができます。この特異性は、信じられないほど広範囲の病原体を標的にして中和する適応免疫システムの能力の基礎となります。
Fc 地域: エフェクター機能ファシリテーター

抗体の定常領域: アイソタイプの決定と免疫応答の調節
抗体の定常領域、特に Fc 部分は、抗体のアイソタイプを決定する上で重要な役割を果たします。この領域は、可変領域と比較して変動が少なく、クラス固有の機能に安定したフレームワークを提供します。抗体のアイソタイプは、抗体が次のような免疫系の他の要素とどのように相互作用するかに影響します。
エフェクター細胞の動員: 免疫細胞上のさまざまな Fc 受容体は、特定の抗体アイソタイプに対して異なる親和性を持ち、これらの細胞を感染部位に動員する抗体の能力に影響を与えます。
補体系の活性化: 特定の抗体アイソタイプは、病原体の破壊につながる一連の酵素反応である補体カスケードを開始できます。
経胎盤移行: IgG 抗体の Fc 領域は、胎盤を通過する抗体の移行を促進し、胎児に受動免疫を提供します。
定常領域の構造的および機能的特性は、免疫防御における抗体の全体的な有効性に不可欠であり、病原体の直接的な中和と広範な免疫応答の調整の両方に影響を与えます。
定常領域の機能
Fc 受容体への結合: 免疫細胞上の Fc 受容体は定常領域を認識し、抗体依存性細胞傷害 (ADCC) を促進します。
補体活性化: 定常領域は古典的な補体経路を開始し、病原体の溶解を引き起こします。
新生児免疫: 特定の定常領域により抗体が胎盤を通過できるようになり、胎児に受動免疫が提供されます。
抗体軽鎖
免疫グロブリンとしても知られる抗体分子は、適応免疫システムの典型的な構成要素です。それらは驚くべき特異性と多様性を示し、膨大な数の病原体や外来分子を特定して無力化することができます。この機能の中心となるのは、カッパ (κ) とラムダ (λ) という 2 種類の軽鎖です。これらは、ヒトの抗体内におよそ 2:1 の比率で存在します。これらの軽鎖は重鎖とともに抗体の抗原結合部位を形成し、その独特の抗原結合親和性と特異性を決定します。この複雑な集合体は、抗体の構造的完全性を支えるだけでなく、無数の抗原を認識して対抗する免疫系の能力において極めて重要な役割を果たします。
軽鎖の種類
カッパ (κ) チェーン
カッパ鎖は、ヒト抗体に見られる主なタイプの軽鎖です。各カッパ鎖は、可変 (V) ドメインと定常 (C) ドメインで構成されます。 V ドメインは抗原結合部位に寄与し、C ドメインは免疫系の他の構成要素と相互作用します。カッパ鎖をコードする遺伝子座はかなりの多様性を示し、これが抗体に見られる抗原結合特異性と多様性の源となっています。この多様性により、それぞれが固有の抗原を標的とすることができる、膨大な抗体のレパートリーの生成が可能になります。
ラムダ (λ) チェーン
ラムダ鎖は、カッパ鎖ほど一般的ではありませんが、免疫応答において同様に重要な役割を果たします。カッパ鎖と同様に、ラムダ鎖は、抗体の抗原結合機能とエフェクター機能に寄与する可変ドメインと定常ドメインで構成されています。ラムダ鎖遺伝子も大きな変動性を示し、一連の抗原に対して高い特異性を備えた抗体を生成する免疫系の能力にさらに寄与しています。

表 1: カッパ軽鎖とラムダ軽鎖の比較
特徴 | カッパ(κ)チェーン | ラムダ (λ) チェーン |
分布 | ヒトの抗体の約 60% | ヒトの抗体の約 40% |
遺伝子座 | 2 番染色体上の κ 遺伝子座 | 22番染色体上のλ遺伝子座 |
チェーンの長さ | やや短め | やや長め |
役割と機能
軽鎖の主な機能は、抗体の抗原結合部位に寄与し、抗体が抗原を特異的に認識して結合できるようにすることです。この抗原結合能力は、免疫応答における抗体の役割の基礎であり、病原体を中和したり、病原体にタグを付けて破壊したり、その活性をブロックしたりすることができます。さらに、軽鎖の多様性によってもたらされる抗原認識の特異性は、自己と非自己を区別する免疫系の能力にとって重要であり、感染症と効果的に闘いながら自己免疫反応を防止します。
腫瘍関連抗原: がん免疫学における重要性
腫瘍関連抗原 (TAA) は、腫瘍細胞の表面に発現するタンパク質です。それらは、抗体媒介反応の標的として免疫系によって認識されます。
腫瘍関連抗原 (TAA) の状況を理解することは、がん免疫療法を進歩させるために不可欠です。ここでは、過剰発現抗原、変異抗原、および癌精巣抗原という 3 つの主要なタイプの TAA についてさらに深く掘り下げ、明確にするために構造化された情報を含む簡潔な概要を提供します。

腫瘍関連抗原の種類
腫瘍関連抗原 (TAA) の状況を理解することは、がん免疫療法を進歩させるために不可欠です。ここでは、TAA の 3 つの主要なタイプについて詳しく説明します。
過剰発現した抗原
変異した抗原
癌-精巣抗原、
1. 過剰発現した抗原
正常な細胞タンパク質と比較して、がん細胞内にはるかに高いレベルで存在する正常な細胞タンパク質。それらの過剰発現は癌細胞の悪性表現型に寄与する可能性があり、免疫療法の標的となります。
例と意義
HER2/neu: 特定の種類の乳がんで過剰発現され、モノクローナル抗体 (例: トラスツズマブ) の標的となります。
CD20: B 細胞の表面に存在し、非ホジキンリンパ腫をリツキシマブで標的とします。
表 1: 過剰発現された抗原
抗原 | がんの種類 | 治療標的 |
HER2/ノイ | 乳癌 | トラスツズマブ |
CD20 | 非ホジキンリンパ腫 | リツキシマブ |
2. 変異抗原
腫瘍細胞ゲノムの突然変異から生じる抗原。これらの変異は、免疫系によって異物として認識される異常なタンパク質の生成を引き起こす可能性があり、標的療法の基礎となります。
例と意義
EGFRvIII: 神経膠芽腫のサブセットで変異した EGF 受容体の変異体で、ワクチン療法の標的となります。
BRAF V600E: 低分子阻害剤 (ベムラフェニブなど) の標的となる黒色腫の変異。
例と意義
EGFRvIII: 神経膠芽腫のサブセットで変異した EGF 受容体の変異体で、ワクチン療法の標的となります。
BRAF V600E: 低分子阻害剤 (ベムラフェニブなど) の標的となる黒色腫の変異。
表 2: 変異抗原
抗原 | がんの種類 | 治療標的 |
EGFRvIII | 膠芽腫 | ワクチン療法 |
BRAF V600E | 黒色腫 | ベムラフェニブ |
3. 癌-精巣抗原
TAA の一種。通常は雄の生殖系列細胞 (精巣など) でのみ発現しますが、さまざまな腫瘍で異常に発現します。これらは免疫原性があり、正常組織での発現が制限されているため、がんワクチンやその他の免疫療法の有望な標的と考えられています。
例と意義
MAGE-A3: ワクチン療法の対象となる黒色腫、肺、その他のがんで発現します。
NY-ESO-1: T 細胞ベースの治療法やワクチンの標的となる、さまざまながんで広範に発現します。

表 3: 癌-精巣抗原
抗原 | がんの種類 | 治療標的 |
メイジ-A3 | 黒色腫、肺がん | ワクチン療法 |
NY-ESO-1 | さまざまながん | T細胞療法、ワクチン |
各タイプの TAA は、がんを正確に標的とする独自の機会を提供します。過剰発現抗原はタンパク質レベルの量的な違いに基づいたターゲティングを可能にし、変異抗原は癌特異的変異に由来する特異性を提供し、癌精巣抗原は正常組織での発現が制限された標的を提示します。これらの抗原の理解と標的化の進歩は、より効果的で毒性の少ないがん治療を開発する鍵となります。
結論
多様な構造と機能を持つ抗体は、がん細胞などの病原体に対する免疫防御の最前線にあります。軽鎖の特異性、定常領域のエフェクター機能、および腫瘍関連抗原を標的とする能力は、免疫応答の複雑さと効率を示しています。研究が進むにつれて、これらの成分をより詳細に理解することで、感染症やがんに対する治療戦略が強化されるでしょう。
参考文献
Janeway, C.A.、Travers, P.、Walport, M.、Shlomchik, M.J. (2001)。免疫生物学: 健康と病気における免疫システム。第5版。ガーランドサイエンス。
マーフィー、K.、ウィーバー、C. (2016)。ジェインウェイの免疫生物学。第9版。ガーランドサイエンス。
Klein、J.、Sato、A. (2000)。 HLA システム。ニューイングランド医学ジャーナル、343(10)、702-709。
パードール、D.M. (2012)。がん免疫療法における免疫チェックポイントの遮断。 Nature Reviews Cancer、12(4)、252-264。
Weiner, L.M.、Surana, R.、および Wang, S. (2010)。モノクローナル抗体: がん免疫療法のための多用途プラットフォーム。 Nature Reviews Immunology、10(5)、317-327。
大橋、追伸(2002)。腫瘍免疫と自己免疫: バランスをとる行為。自然免疫学、3(4)、337-339。
C.J. メリーフ、T. ヴァン ホール (2012)。治療用のがんワクチン。臨床研究ジャーナル、122(10)、3395-3400。
クーリー、P. G.、ヴァン デン アインデ、B. J.、ファン デル ブリュッゲン、P.、およびブーン、T. (2014)。 T リンパ球によって認識される腫瘍抗原: がん免疫療法の中核。 Nature Reviews Cancer、14(2)、135-146。
16th Dec 2024
Recent Posts
-
がんの共通特性 | Assay Genie
シェーン・ヒューストン、クイーンズ大学ベルファスト校博士候補がんは人類にとって古くからの敵です。異常細胞の制御不能な増殖は、歴史を通じて人間の健康に影を落としてきました。が …11th Mar 2025 -
がん治療薬としてのSTING活性剤
STING (インターフェロン遺伝子刺激因子) 経路は、がん細胞や DNA ウイルスに対する自然免疫システムの反応において極めて重要な役割を果たします。STING 活性剤を …8th Mar 2025 -
Nod 様受容体シグナル伝達経路: 自然免疫の要
病原体に対する主な防御線である自然免疫システムは、さまざまな細胞および分子メカニズムで構成されています。これらのうち、Nod 様受容体 (NLR) シグナル伝達経路は重要な …8th Mar 2025