ミクログリア細胞の機能と神経変性疾患における役割
重要なポイント:
ミクログリアとは何ですか?
ミクログリアの機能とは何ですか?
ミクログリアは中枢神経系内で無数の機能を果たし、神経組織全体の健康と機能に貢献します。ミクログリアは、損傷、感染、または異常な変化の兆候がないか中枢神経系を常に監視しています。神経伝達物質やサイトカインなどのさまざまなシグナルを検出して反応する能力により、障害に対して機敏に反応することができます。さらに、ミクログリアは、食作用を介した細胞破片、損傷したニューロン、有毒タンパク質凝集体の除去において重要な役割を果たします。ミクログリアはこれらの有害物質を効率的に除去することで、清潔で健康な神経環境の維持に役立ちます。
ミクログリアの種類は何ですか?
ミクログリア細胞はさまざまな形態学的および機能的状態を示し、中枢神経系における多様な役割に寄与しています。 1 つの分類体系では、いくつかの異なるタイプのミクログリアが認識されます。ミクログリア細胞には、アメーバ状ミクログリア、分枝状ミクログリア、反応性ミクログリアの 3 つの主要なタイプがあります。ミクログリア細胞の顕著な可塑性により、ミクログリア細胞は微小環境に適応して応答することができ、免疫監視、神経炎症、組織修復、およびシナプスのリモデリングに貢献します。
アメーバ様ミクログリア:
アメーバ状ミクログリアは、収縮した突起を伴う丸い形態を特徴とする活性化状態を表します。それらは移動性と貪食性が高く、細胞残骸を除去し、組織修復を促進する上で重要な役割を果たします。アメーバ様ミクログリアは通常、発生の初期中、または損傷や炎症に反応して観察されます。これらの動的細胞は環境の変化に迅速に反応し、休止状態から活性化状態に移行します。そのアメーバ状の形状により、組織内を効率的に移動して破片を飲み込み、損傷や炎症の解決に貢献します。アメーバ状ミクログリアは、さまざまなシグナル伝達分子や炎症誘発性サイトカインを放出し、中枢神経系内の免疫応答に関与します。
分岐ミクログリア:
分枝状ミクログリアは、休止期ミクログリアとしても知られ、健康な中枢神経系におけるミクログリアのベースライン状態です。それらは高度に分岐した形態を持ち、細胞体から多数の突起が伸びています。枝分かれしたミクログリアは神経環境を継続的に監視し、恒常性の維持を確保します。この静止状態では、免疫監視において重要な役割を果たし、異常がないか周囲の神経組織を積極的に調査します。分枝状ミクログリアは常にニューロンや他のグリア細胞と相互作用し、ニューロンの健康に貢献し、脳の正常な機能をサポートします。彼らは休んでいると考えられていますが、活性化された状態に移行することによって、あらゆる摂動に迅速に反応する能力を保持しています。
反応性ミクログリア:
何がミクログリアを活性化するのでしょうか?
ミクログリアの活性化は、病原体関連分子パターン (PAMP) や損傷関連分子パターン (DAMP) を含むさまざまな刺激に応答して起こります。ミクログリアの活性化には、PAMP、DAMP、およびそれらの対応する受容体の間の複雑な相互作用が関与し、細胞内シグナル伝達経路と遺伝子発現の変化を引き起こします。活性化プロセスは、状況および微小環境に応じて、炎症誘発性 (M1) 表現型または抗炎症性および組織修復 (M2) 表現型のいずれかをもたらします。
ミクログリア活性化のマーカー
ミクログリアの活性化は、CNS 内の免疫応答において重要な役割を果たしており、さまざまな神経変性疾患と関連しています。活性化されたミクログリアを特定し特徴付けるために、いくつかのマーカーが一般的に使用されます。活性化されたミクログリアを検出するために使用できるマーカーは多数あります。これらのマーカーには、CD11b、CD68、Iba-が含まれます。活性化されたミクログリアは、陽電子放射断層撮影法 (PET)、磁気共鳴画像法 (MRI)、単一光子放射型コンピューター断層撮影法 (SPECT) などのイメージング技術を使用して検出できます。
ミコグリアと脳の健康
ミクログリアの機能の重要な側面の 1 つは、ミクログリアの貪食と除去の熟練度です。ミクログリアは、細胞破片、アポトーシス細胞、および毒性タンパク質凝集体を脳から飲み込んで除去する役割を担っています。この貪食活動は、健康な神経環境を維持し、潜在的に有害な物質の蓄積を防ぐために不可欠です。ミクログリアは細胞の老廃物を効率的に除去することで、CNS の全体的な健康と機能に貢献します。
ミクログリアは、CNS損傷または神経変性プロセスに応答して、神経保護および組織修復メカニズムに貢献します。それらは、神経細胞の生存、組織の治癒、再生を促進する成長因子、栄養因子、抗炎症分子を放出します。局所微小環境を調節するミクログリアの能力は、損傷または損傷後のニューロンの回復と修復をサポートします。

ミコグリアと神経変性
アルツハイマー病、パーキンソン病、多発性硬化症などの神経変性疾患は、ニューロンの機能と構造が進行的に失われることを特徴としています。近年、これらの疾患の病因におけるミクログリアの役割が大きな注目を集めています。ミクログリアは、病気の進行における主要なプレーヤーとして、また潜在的な治療標的として、神経変性プロセスに積極的に関与しています。
アルツハイマー病におけるミクログリア
パーキンソン病におけるミクログリア
パーキンソン病では、ニューロン内にミスフォールドされたα-シヌクレインタンパク質が蓄積するとレビー小体の形成が起こり、ニューロンの機能不全と死を引き起こします。ミクログリアはこの病気において二重の役割を果たします。最初に、ミクログリアは、α-シヌクレイン凝集体を貪食して除去することによって防御反応を示すことができます。しかし、ミクログリアの慢性的な活性化と神経毒性物質の放出は、神経炎症の一因となり、神経損傷を悪化させます。ミクログリア、α-シヌクレインの病理、およびニューロン喪失の間の複雑な相互作用を理解することは、ミクログリアの機能を調節し、疾患の進行を遅らせるための戦略を開発するために非常に重要です。
多発性硬化症におけるミクログリア
多発性硬化症 (MS) は、慢性炎症、脱髄、CNS への免疫介在性損傷を特徴とします。ミクログリアおよび他の免疫細胞は、MS の発症において重要な役割を果たします。活性化されたミクログリアは炎症誘発性サイトカインやケモカインを放出することで神経炎症に寄与し、免疫細胞の補充と活性化を引き起こします。それらはミエリン残骸の除去にも関与します。しかし、ミクログリアの持続的な活性化は炎症反応を永続させ、さらなる組織損傷を引き起こす可能性があります。
神経変性疾患におけるミクログリアの治療可能性
ミクログリアは、神経変性疾患における治療介入の興味深い標的として浮上しています。それらの動的かつ複雑な機能は、潜在的な治療戦略への道を提供します。 1 つのアプローチは、ミクログリアの活性化を調節することです。ミクログリアを炎症促進性(M1 様)表現型から抗炎症性(M2 様)表現型に移行させることは、慢性神経炎症を緩和し、神経毒性を軽減する可能性を秘めています。この調節を達成するために、特定のシグナル伝達経路を標的とする戦略、または免疫調節剤を利用する戦略が検討されています。
関連キット
 |
 |
 |
Recent Posts
-
がんの共通特性 | Assay Genie
シェーン・ヒューストン、クイーンズ大学ベルファスト校博士候補がんは人類にとって古くからの敵です。異常細胞の制御不能な増殖は、歴史を通じて人間の健康に影を落としてきました。が …11th Mar 2025 -
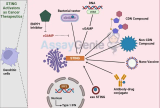
がん治療薬としてのSTING活性剤
STING (インターフェロン遺伝子刺激因子) 経路は、がん細胞や DNA ウイルスに対する自然免疫システムの反応において極めて重要な役割を果たします。STING 活性剤を …8th Mar 2025 -
Nod 様受容体シグナル伝達経路: 自然免疫の要
病原体に対する主な防御線である自然免疫システムは、さまざまな細胞および分子メカニズムで構成されています。これらのうち、Nod 様受容体 (NLR) シグナル伝達経路は重要な …8th Mar 2025