プロテインキナーゼ:概要、分類、および治療の可能性
重要なポイント:
キナーゼとは何ですか?その機能、種類、構造を理解する
プロテインキナーゼの機能

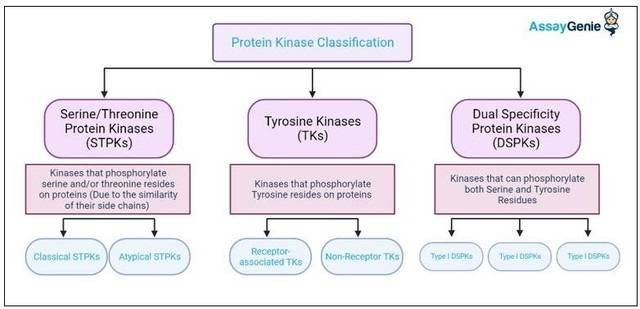
プロテインキナーゼの分類

セリン/スレオニン特異的プロテインキナーゼ (STPK)
チロシン特異的プロテインキナーゼ (TK)
二重特異性プロテインキナーゼ (DSPK)
プロテインキナーゼの構造
シグナル伝達におけるプロテインキナーゼ
プロテインキナーゼの制御
プロテインキナーゼの制御は、その活性と機能を正確に制御するための非常に複雑なプロセスです。さまざまなメカニズムがプロテインキナーゼの制御に寄与し、動的で状況に依存したシグナル伝達を可能にします。一般的な調節様式の 1 つは、リン酸化 (マグネシウム イオンが必要で、酵素への結合に関して ATP と競合する化合物によって阻害される)、アセチル化、またはユビキチン化などの翻訳後修飾を介するもので、キナーゼを活性化または不活化することができます。さらに、プロテインキナーゼはアロステリック制御を受ける可能性があり、小分子または他のタンパク質の結合によってその活性が調節されます。アクチベーターはプロテインキナーゼの活性を増加させますが、インヒビターはその活性を減少させます。プロテインキナーゼに結合するリガンドは、天然リガンド (ATP など) または合成リガンド (薬物など) のいずれかです。 ATP の濃度もキナーゼ活性に影響します。
調節されていないプロテインキナーゼ活性に関連する疾患
プロテインキナーゼは、細胞シグナル伝達経路の主要な調節因子として、正常な細胞機能を維持する上で重要な役割を果たします。しかし、遺伝子変異、発現レベルの変化、または異常な活性化機構によって、これらのキナーゼが調節不全になると、衰弱性疾患の発症や進行に寄与する可能性があります。プロテインキナーゼは、細胞シグナル伝達経路の重要な調節因子として重要な役割を果たします。正常な細胞機能の維持に。しかし、遺伝子変異、発現レベルの変化、または異常な活性化機構によって、これらのキナーゼが調節不全になると、衰弱性疾患の発症および進行に寄与する可能性があります。

プロテインキナーゼ阻害剤とその治療の可能性
プロテインキナーゼ阻害剤とは何ですか?
プロテインキナーゼ阻害剤は、プロテインキナーゼの活性を特異的に標的にしてブロックする薬物の一種です。低分子阻害剤とペプチド阻害剤の 2 つの主なカテゴリがあります。小分子阻害剤は標準的な化学療法薬として使用されますが、ペプチド阻害剤は臨床試験中です。
これらの阻害剤はどのように作用するのでしょうか?
プロテインキナーゼ阻害剤は、キナーゼの活性部位または他の領域に結合することで作用し、ATP および基質タンパク質との相互作用を防ぎます。このキナーゼ活性の阻害により、キナーゼの機能に依存するシグナル伝達経路や細胞プロセスが混乱する可能性があります。これらの阻害剤は、疾患経路に関与する特定のプロテインキナーゼを選択的に標的とすることで、異常なシグナル伝達を調節し、正常な細胞機能を回復する可能性をもたらします。
さまざまな病気における治療の可能性
プロテインキナーゼ阻害剤はがん治療に革命をもたらし、精密医療の大幅な進歩につながりました。これらは、がん細胞の増殖と生存を促進するキナーゼを特異的に阻害できるため、標的療法の基礎となっています。さらに、これらの阻害剤は、自己免疫疾患、神経変性疾患、代謝障害など、キナーゼシグナル伝達の調節不全を特徴とする他の疾患の治療にも期待されています。いくつかの例は次のとおりです。
プロテインキナーゼ阻害剤は、さまざまな疾患領域にわたって大きな治療可能性を秘めています。プロテインキナーゼ阻害剤の開発と応用は、各疾患に特有のキナーゼ活性の調節異常に対するより深い理解によって推進され、標的を絞った介入と個別の治療アプローチが可能になります。ただし、プロテインキナーゼ阻害剤は顕著な治療可能性を示している一方で、課題が残っていることに留意することが重要です。薬剤耐性、オフターゲット効果、および特定の患者集団における限定的な有効性は、現在研究と改善が行われている分野です。それにもかかわらず、プロテインキナーゼ阻害剤は引き続き医薬品開発の有望な分野であり、さまざまな疾患に個別化され、標的を絞った治療介入への新たな道を提供します。
関連製品
 |
 |
 |
Recent Posts
-
がんの共通特性 | Assay Genie
シェーン・ヒューストン、クイーンズ大学ベルファスト校博士候補がんは人類にとって古くからの敵です。異常細胞の制御不能な増殖は、歴史を通じて人間の健康に影を落としてきました。が …11th Mar 2025 -
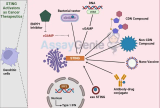
がん治療薬としてのSTING活性剤
STING (インターフェロン遺伝子刺激因子) 経路は、がん細胞や DNA ウイルスに対する自然免疫システムの反応において極めて重要な役割を果たします。STING 活性剤を …8th Mar 2025 -
Nod 様受容体シグナル伝達経路: 自然免疫の要
病原体に対する主な防御線である自然免疫システムは、さまざまな細胞および分子メカニズムで構成されています。これらのうち、Nod 様受容体 (NLR) シグナル伝達経路は重要な …8th Mar 2025